Texto Bruno Carbinatto Ilustração Felipe Del Rio Design Caroline Aranha Edição Rafael Battaglia
Nota: a versão impressa desta reportagem foi publicada dias antes da aprovação do lenacapavir no Brasil pela Anvisa.
O ano é 1981, e um artigo publicado pelo Centro de Controle e Prevenção de Doenças dos EUA intriga a comunidade científica global. Nele, os pesquisadores descreveram cinco casos de homens jovens com pneumonia causada pelo fungo Pneumocystis. É uma doença bastante rara – até então, só era registrada em pacientes muito imunossuprimidos, como em quadros avançados de câncer. Do contrário, nosso sistema imunológico dá conta de combater o patógeno.
Siga
Dois dos doentes morreram antes mesmo de o artigo terminar de ser escrito. Por quê?
O que deixou suas defesas em frangalhos? Demorou dois anos para que o causador da Síndrome da Imunodeficiência Adquirida (Aids) fosse descoberto: o Vírus da Imunodeficiência Humana (HIV), um parasita que pulou dos macacos para os humanos no meio do século 20 e se tornou mestre em infectar nossas células.
Esses foram os primeiros capítulos de uma pandemia que já infectou 91 milhões no mundo e ceifou a vida de 44 milhões (o termo “epidemia” também pode ser utilizado, já que, apesar de global, os casos são concentrados). A doença levou ícones como Freddie Mercury, Cazuza e Renato Russo, impulsionou uma onda de discriminação e preconceito e deixou uma marca especialmente sombria na história da comunidade LGBT+.
Faz tempo, entretanto, que ter HIV deixou de ser uma sentença de morte. Graças aos medicamentos antirretrovirais, um paciente tem expectativa e qualidade de vida quase idênticas a alguém sem o vírus.
Além disso, mesmo que a vacina seja um sonho distante, criamos uma maneira medicamentosa de prevenir a infecção (além dos métodos clássicos, como o uso de preservativos): é a Profilaxia Pré-Exposição (PrEP), um comprimido diário que quase zera as chances de uma pessoa contrair o vírus, mesmo se exposta a situações de risco (sexo sem camisinha ou compartilhar objetos cortantes, por exemplo).
Acabar com a pandemia, porém, ainda está longe de acontecer. Mas, nos últimos anos, demos um passo importante
Em 2024, cientistas anunciaram que um novo medicamento, o lenacapavir, tem quase 100% de eficácia na prevenção de novos casos de HIV. Com o detalhe de que ele funciona com apenas uma injeção semestral. A farmacêutica americana Gilead, veterana em produzir fármacos para a PrEP, foi além e agora testa o lenacapavir num regime de apenas uma injeção por ano. Os resultados são promissores.
Seja semestral (que já sabemos que funciona), seja anual (a ver), o lenacapavir parece ser a melhor arma já criada para frear a pandemia do HIV. Não é uma vacina – ele não produz memória imunológica –, mas age, na prática, como uma.
Por isso mesmo, o prestigiado periódico Science elegeu o medicamento como a “descoberta do ano” em 2024 (em 2023, quem levou esse título foram os análogos de GLP-1, como o Ozempic e o Mounjaro, que estão revolucionando a luta contra a obesidade). No meio de 2025, o lenacapavir recebeu aprovação nos EUA. Pouco depois, a OMS passou a recomendá-lo. Na reta final do ano, a injeção começou a ser aplicada em alguns países africanos. E agora, no início de 2026, a Anvisa aprovou o fármaco no Brasil (sob o nome comercial Sunlenca).
O medicamento é descrito como “impressionante”, “revolucionário” e um “divisor de águas” por especialistas. Um outro fármaco do tipo, de aplicação bimestral, também ajudou a inaugurar uma onda de otimismo na comunidade médica. Se usados amplamente, podem iniciar uma nova etapa no combate à Aids, derrubando o número de novos casos. Mais de 1,3 milhão de pessoas contraem o vírus no mundo todos os anos.
A meta da Unaids, a agência da ONU para o HIV, é reduzir esse número para 200 mil novos casos anuais até 2030. Segundo o órgão, esse patamar seria suficiente para fazer com que a doença deixe de ser uma ameaça à saúde pública global.
O lenacapavir, aliado a outras estratégias, torna esse alvo mais realista. Mas ainda há um problemão: garantir que ele chegue às pessoas mais vulneráveis. O HIV afeta com muito mais força os países pobres, especialmente na África Subsaariana, e o seu manejo depende de ajuda financeira dos países ricos.
No segundo mandato de Trump, porém, a torneira americana fechou. O sistema de doações e cooperação internacional, que salvou milhões de vidas nas últimas décadas, está em risco de colapsar.
Não só. Mesmo se zerarmos a transmissão do HIV, o problema não acaba: hoje, mais de 40 milhões de pessoas mundo afora vivem com o vírus. A doença é crônica e precisa de tratamento para o resto da vida.
A cura segue furtiva, mas também nessa área há avanços notáveis – um deles, inclusive, feito por cientistas brasileiros. Nas próximas páginas, vamos entender as inovações recentes da ciência para enfrentar um dos inimigos mais ardilosos da saúde pública global.

O beabá da invasão
Vírus são seres incrivelmente simples. Consistem em minúsculos pacotinhos recheados de material genético (RNA ou DNA) e algumas proteínas e gorduras, cuja única função é gerar cópias de si mesmos
Mas há um problema: eles não têm o maquinário necessário para o Control+C, Control+V. É por isso que precisam de um hospedeiro.
Nas nossas células, a receita para criar proteínas está guardada no DNA. O material genético é lido pela organela ribossomo, que junta pecinhas (os aminoácidos) para fazer a molécula descrita.
Os vírus até têm a receita, mas não a cozinha. Por isso, são parasitas, que usam as ferramentas de seus hospedeiros para criar novas cópias de si mesmos (por causa dessa ausência de metabolismo, diga-se, a maioria dos cientistas nem sequer considera os vírus como uma forma de vida).
O HIV, com apenas nove genes (os humanos têm dezenas de milhares), tem um jeito engenhoso de fazer isso. Ele é um retrovírus: consegue se infiltrar no núcleo dos linfócitos T CD4+, peças-chave do sistema imunológico, e colar pedaços de seu próprio material genético no nosso.
Sem notar, o corpo lê a receita viral e produz os ingredientes necessários para formar novos vírions (o nome de cada partícula isolada de HIV). Depois, basta que essas partes se juntem e deixem a célula para colonizar as vizinhas, destruindo-a no processo.
Para isso, o vírus usa algumas enzimas com funções específicas. A transcriptase reversa, por exemplo, tem um papel relevante: transforma o RNA viral, uma fita simples de material genético, em uma fita dupla de DNA – é ela que será inserida no nosso genoma.
Com o tempo, esse ciclo infeccioso mata quase todos os glóbulos brancos do hospedeiro, causando a síndrome que chamamos de Aids. Sem esses glóbulos, agentes vitais do sistema imunológico, os pacientes ficam vulneráveis a infecções diversas. Podem morrer de infecções secundárias simples.
O fato de o HIV se integrar ao nosso DNA é um dos maiores obstáculos para a produção de uma vacina: ainda não descobrimos um jeito de ensinar o sistema imunológico a reconhecê-lo como inimigo. Muitas vacinas tradicionais usam versões inativadas ou enfraquecidas do invasor, mas essa não é uma boa opção contra os retrovírus porque, mesmo todo capenga, ainda há o risco de ele conseguir escrever seu material genético em nossas células, começando um ciclo de infecção. Como se não bastasse, o HIV é altamente mutável e mestre em se esconder das nossas células de defesa.
Depois que os cientistas entenderam os mecanismos do HIV, ficou um pouco mais fácil achar um jeito de brecar a ação de uma ou outra das suas ferramentas moleculares. Foi assim que nasceu o AZT (zidovudina), o primeiro fármaco contra o HIV, em 1987. Ele dificulta a atividade da transcriptase reversa e foi essencial para prolongar a vida dos primeiros pacientes. Mas, sozinho, era pouco eficaz e tinha muitos efeitos colaterais.
O jogo mudou em 1996, quando surgiram outros medicamentos, baseados em mecanismos de ação diversos. Alguns atacam a protease, uma enzima que funciona como uma “tesoura” usada pelo HIV para cortar proteínas grandes em pedaços menores; outros inibem a integrase, responsável por inserir o material genético do vírus no nosso [veja mais no quadro abaixo].
Nascia assim o coquetel: uma mistura de diferentes estratégias para atacar o HIV por várias frentes, garantindo que a maior parte dos patógenos fosse eliminada.
No início, o tratamento era feito com várias pílulas, tomadas diversas vezes ao longo do dia, mas hoje a maioria dos pacientes ingere apenas um comprimido diário (contendo, geralmente, dois ou três medicamentos). Os efeitos colaterais são poucos.

Desde então, pessoas com HIV conseguem reduzir o nível do vírus no sangue a patamares tão baixos que nem sequer são detectáveis nos exames. Na década de 2010, os cientistas confirmaram o chamado “protocolo i=i”: estar indetectável significa também estar intransmissível. Ou seja: um paciente medicado corretamente não passa o vírus para outras pessoas, mesmo no sexo desprotegido.
A próxima inovação veio no campo da prevenção. Desde a década de 1990 os profissionais de saúde sabiam que, em um possível caso de contaminação (contato com sangue de um portador, por exemplo), tomar o coquetel nas primeiras 72 horas preveniria a infecção. Isso porque os medicamentos neutralizam o HIV antes que ele possa se instalar de vez nas células. É a chamada PEP (profilaxia pós-exposição).
Daí veio a ideia: se alguém sem o vírus tiver sempre uma concentração alta dos medicamentos anti-HIV no sangue, o patógeno nunca vai conseguir se fixar. A pessoa fica, em tese, imune.
Em 2012, nasce a PrEP: um medicamento contendo antirretrovirais que é tomado diariamente por indivíduos sem HIV para a prevenção.
A PrEP é recomendada especialmente para pessoas mais vulneráveis – homens que fazem sexo com homens (essa é a definição médica, para evitar rótulos), profissionais do sexo, usuários de drogas injetáveis etc. No Brasil, é oferecida pelo SUS desde 2017. Hoje, são 140 mil pessoas protegidas, quase o triplo do registrado em 2022 (50 mil).
Se usada corretamente, a PrEP tem eficácia altíssima, de mais de 99%, com pouquíssimos efeitos colaterais.
Só na cidade de São Paulo, por exemplo, os novos casos de HIV caíram 54% entre 2016 e 2023, de 3.761 para 1.705. A queda é creditada a vários motivos, claro, mas a PrEP é, sem dúvida, um deles.
Só que há um problema nessa estratégia: a adesão. O usuário precisa tomar um comprimido por dia, e isso nem sempre é fácil. Esquecimento é uma falha comum, mas não só. Existe o estigma, a vergonha de ser visto com as pílulas, a necessidade de explicar para os parceiros…
Além disso, nem sempre o acesso é fácil – o Brasil é referência nesse quesito, distribuindo o medicamento de graça, mas o epicentro da pandemia de HIV está nos países pobres da África Subsaariana, com frágeis sistemas de saúde.
É por isso que, na prática, a eficácia do uso da PrEP varia muito e nunca atinge os 99%. Facilitar a adesão é a chave para turbinar o método de prevenção. Mas como?
Nos últimos anos, uma inovação veio para tentar resolver esse problema. Em 2021, os EUA aprovaram o cabotegravir na versão injetável. Trata-se de um antirretroviral que também pode ser tomado para tratar o HIV, mas que, nessa versão, é focado em prevenir a infecção.
Uma injeção a cada dois meses insere uma grande quantidade do medicamento no músculo do paciente; nos próximos 60 dias, a substância vai sendo liberada aos poucos no sangue, garantindo a prevenção contra o vírus durante o período.
É uma PrEP injetável, mais prática e fácil de ser aplicada em grandes populações – basta uma visita bimestral a um serviço de saúde e uma picadinha nos glúteos ou na perna –, o que poderia driblar os problemas de adesão.
Por aqui, o cabotegravir foi aprovado pela Anvisa em 2023 e está disponível no serviço privado, mas o preço é (bem) salgado: cada dose chega a custar R$ 4 mil. Há uma avaliação para agregá-lo ao SUS, ainda sem prazo.
De qualquer forma, ele já é uma grande aposta para prevenir milhões de novos casos. Mais recentemente, um outro medicamento surgiu, e com um mecanismo ainda mais notável.

Prazer, lenacapavir
No centro do HIV está uma estrutura chamada capsídeo, uma fina malha proteica que envolve o material genético e algumas das enzimas do vírus, protegendo-o.
Por muito tempo, cientistas acreditavam que o tal capsídeo era uma parte estrutural do vírus, uma camada de proteção sem grandes funções em seu ciclo de replicação. Além disso, ele é estável, difícil de ser atacado.
Por isso, a maioria das linhas de pesquisa deixou o capsídeo de lado e focou em inibir a ação das enzimas do HIV, como já vimos; elas são menores, mais simples, e é mais fácil encontrar moléculas que interagem com elas. Alguns virologistas, porém, continuaram a acreditar que ele era um alvo viável.
O capsídeo é formado por partículas de uma única proteína, a p24. Essas pecinhas se juntam em grupos de seis (os hexâmeros) ou, mais raramente, de cinco (os pentâmeros). Esses bloquinhos, por sua vez, ligam-se uns aos outros;
O resultado desse Lego é uma grande malha proteica em formato de cone, que envolve o RNA viral do HIV. Essa camada é resistente, mas flexível – uma característica importante para que o vírus consiga se infiltrar nas células.
Em 2012, um dos vários compostos testados pela farmacêutica Gilead mostrou ser capaz de atacar essa malha. O lenacapavir é uma molécula bem pequena, que consegue se ligar a cada uma das proteínas p24 que formam os hexâmeros e os pentâmeros. Ele funciona como um grampo: “aperta” essas estruturas, deixando o capsídeo mais rígido.
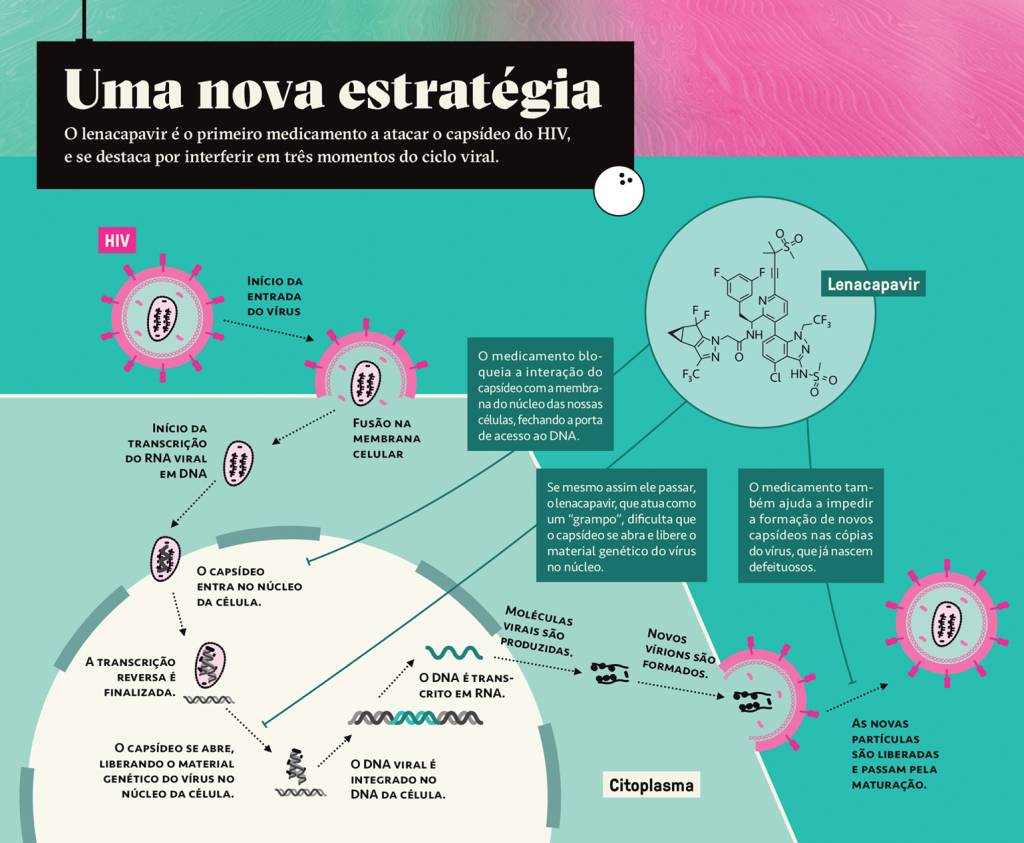
A vantagem desse medicamento, que o torna tão revolucionário, é que ele atrapalha o HIV em três pontos distintos de seu ciclo de replicação.
Primeiro, o capsídeo precisa entrar no núcleo da célula do hospedeiro (onde fica o DNA) para liberar o seu material genético viral. Isso é possível porque a estrutura se liga a duas proteínas específicas da membrana nuclear, que abrem a porta para o vírus. Acontece que o lenacapavir fica alojado justamente na mesma região que precisa interagir com essas guardiãs da porteira, dificultando essa ligação. É uma tranca extra, que deixa o vírus para fora do núcleo.
Caso esse mecanismo falhe e o capsídeo consiga passar, tudo bem: o medicamento age também na próxima etapa. Uma vez lá dentro, a malha proteica precisa se desfazer para liberar o material genético do vírus. Mas lembre- -se: o lenacapavir é tipo um grampo – que impede o capsídeo de se abrir.
O remédio age também num terceiro ponto. Mesmo que o vírus consiga criar cópias de seu material genético, ele ainda precisa fabricar novas malhas para seus clones. Aí entra, outra vez, a capacidade do lenacapavir de enrijecer a estrutura proteica, dificultando a sua formação. Game over para o capsídeo, o que inviabiliza novas cópias de HIV. [Veja no gráfico abaixo.]
O lenacapavir é, por ora, o único “inibidor de capsídeo” aprovado. É um mecanismo de ação novo, útil para combater vírus que já criaram resistência às alternativas clássicas.
A molécula foi criada como um tratamento para quem já tem HIV, e também é usada dessa forma, mas ela brilhou mesmo no campo da prevenção. Em 2024, saíram os resultados de dois testes do medicamento como PrEP. Em ambos, o remédio foi administrado em injeções semestrais. Nessa estratégia, a substância fica alojada no tecido adiposo e é, aos poucos, liberada no corpo.
O primeiro estudo envolveu 5.338 jovens mulheres na África do Sul e em Uganda, das quais 2.134 receberam o lenacapavir via seringa. As outras tomaram a PrEP por via oral. No grupo das pílulas, houve infecções (não porque os comprimidos não funcionem, mas porque seu uso foi inconstante). Já no grupo da injeção, nenhum caso de HIV foi registrado.
Na segunda pesquisa, a alta eficácia do medicamento se repetiu: em um grupo de mais de 3 mil pessoas em diversos países (inclusive no Brasil), só dois casos de HIV foram detectados entre os que tomaram lenacapavir.
Uma eficácia que se aproxima dos 100% impressionou até os mais otimistas dos especialistas; em geral, esse é um número que não se costuma observar nem nas melhores vacinas.
O lenacapavir já entrou para o rol das inovações na batalha contra o HIV, ao lado da PrEP oral de 2012 e do coquetel antirretroviral de 1996. “Se a gente tiver acesso a esse medicamento, sobretudo no serviço público de saúde, vamos diminuir muito o número de novas infecções”, diz Paulo Abrão Ferreira, professor de Infectologia da Universidade Federal de São Paulo (Unifesp).
Modelos epidemiológicos mostram que tanto o lenacapavir como o cabotegravir podem prevenir centenas de milhares de novos casos todos os anos; nos cenários mais otimistas, podem ser a arma que faltava para acabarmos com a pandemia num futuro não tão distante.
Para isso, contudo, as agulhas precisam chegar às populações mais vulneráveis.

Vai e volta
65% das pessoas com HIV estão na África. O sul do continente é especialmente afetado: na África do Sul, quase um quinto dos adultos têm o vírus; veja abaixo.

Nessas regiões, grande parte dos esforços – remédios, testagem, PrEP etc. – precisa ser custeada por ajuda humanitária e coordenada por ONGs, organizações internacionais e países ricos.
Historicamente, os EUA são um doador importante: em 2003, George W. Bush fundou uma agência, a PEPFAR, focada em combater o HIV nos países pobres. Por ano, a PEPFAR gasta US$ 6 bilhões – o que corresponde à metade da grana internacional destinada à luta contra a Aids em nações vulneráveis.
A PEPFAR sempre foi referência, mas isso pode estar prestes a mudar. Logo no primeiro dia de seu segundo mandato, em janeiro de 2025, Donald Trump congelou todo o financiamento da agência. A medida fazia parte de um esforço maior do governo em diminuir os gastos públicos e reduzir as doações americanas para outros países.
A reação da comunidade internacional foi de choque e revolta; o congelamento significava que pessoas poderiam morrer por falta de atendimento. A pressão foi tanta que, em fevereiro, o governo emitiu uma aprovação emergencial para vários dos gastos bloqueados, que permanecem ativos.
No entanto, o financiamento não voltou 100% – na verdade, ainda há confusão sobre o que continua e o que foi limado. Jornais relatam que alguns serviços de saúde em países pobres precisaram fechar porque o dinheiro não está chegando.
A postura do governo americano acendeu um enorme alerta entre especialistas em saúde pública, justamente quando o lenacapavir despontava como uma arma com grande potencial. E olha que, até então, o cenário era positivo: a farmacêutica Gilead, que é dos EUA e detém a patente do medicamento, anunciou em 2024 um acordo com seis empresas para fabricar a versão genérica, que será vendida em mais de 120 países de baixa renda.

É algo incomum: em geral, medicamentos levam muitos anos até ganharem a versão barata e acessível. A própria Gilead já foi alvo de muita pressão e críticas na última década, já que ela produziu a primeira PrEP oral, que só ganhou um genérico em 2020, oito anos após sua aprovação.
Nos EUA, o lenacapavir injetável chega a custar US$ 28 mil por ano para cada paciente. A versão genérica, dependendo da demanda, pode sair por só US$ 40 anuais. A Gilead se comprometeu a vender, sem margem de lucro, doses suficientes para tratar 2 milhões de pessoas em países pobres até que a versão genérica fique pronta.
O problema: o acordo, firmado no governo Biden, previa que metade desse total seria pago pelos EUA (a outra metade viria de um fundo internacional, do qual os EUA também são parte relevante). Só que aí Trump veio e cancelou tudo.
De novo, a pressão foi forte e fez o governo voltar atrás e liberar a grana. No final de 2025, as primeiras mil doses do lenacapavir pagas com dinheiro americano chegaram à Zâmbia e a Essuatíni.
Mesmo assim, o futuro do programa é incerto. Os EUA já disseram ter planos de extinguir a PEPFAR e substituí-la por um outro órgão, cujo escopo e objetivos ainda carecem de detalhes.
Além disso, Trump insiste na ideia de que a distribuição do lenacapavir deveria ser focada em mulheres grávidas, a fim de eliminar a transmissão vertical do vírus (de mãe para filho), enquanto especialistas defendem que a aplicação precisa ser mais generalizada para ter um efeito.
Esse vaivém do governo americano é só um dos desafios no caminho do lenacapavir. O outro é a questão do preço em países de renda média, como Brasil e México. Ficamos de fora do acordo dos genéricos firmado pela Gilead, que focou nos países mais pobres.
Agora que o fármaco foi aprovado no Brasil, o ideal seria incluí-lo no SUS, assim como o cabotegravir, mas o custo deve ser um desafio grande.
Isso não significa que estamos desamparados. O Brasil é referência mundial no combate ao HIV. Fomos o primeiro país a garantir o acesso a antirretrovirais para todos os cidadãos, ainda em 1996.
Em dezembro de 2025, mais uma conquista: o Brasil eliminou a transmissão vertical do HIV, tornando-se o maior país do mundo a atingir esse feito. Além disso, a mortalidade por Aids vem caindo e está no menor patamar da História. São resultados que mesmo países mais ricos não conseguem.
É no Brasil, inclusive, que se desenvolve uma das linhas de pesquisa mais promissoras para a cura definitiva do HIV. Vamos entendê-la.
A cura, ou quase
Em agosto de 2013, a Super publicou uma reportagem de capa com o título “Enfim, a cura da Aids”. A manchete, otimista demais, dizia respeito às descobertas científicas da época sobre o porquê de ser tão difícil eliminar o HIV de vez do corpo, mesmo com antirretrovirais tão eficazes.
O HIV se esconde em refúgios recônditos do nosso corpo. Parte dos linfócitos que ele infecta fica latente, num estado de hibernação. O material genético do vírus já está infiltrado no DNA dessas células, mas a produção de mais vírions só ocorre quando os glóbulos brancos acordam, o que acontece gradualmente.
Isso significa que os medicamentos até conseguem eliminar o vírus do sangue, mas eles sempre voltam a aparecer vindos desses “santuários” virais. Por isso, o tratamento tem que ser constante.
Em 2013, na época da última capa da Super sobre o assunto, uma linha de pesquisa bastante promissora tentava resolver esse problema. Cientistas queriam usar métodos para “acordar” essas células latentes e, logo depois, matá-las, eliminando os últimos reservatórios do vírus no corpo. Daí o otimismo da reportagem.
Infelizmente, essa abordagem não funcionou muito bem, pelo menos não sozinha. Mas ela ainda pode ser a chave. “Desde cedo, a gente percebeu que uma única estratégia isolada não ia funcionar”, diz Ricardo Diaz, professor da Unifesp que coordena uma pesquisa para encontrar uma cura da doença.
A ideia do estudo é combinar medicamentos que revertem a latência do vírus com outras duas estratégias. A primeira é a intensificação do tratamento antirretroviral: usar mais medicamentos para além do coquetel normal (cinco em vez de três, por exemplo), uma artilharia pesada para tentar eliminar todo o HIV.
A segunda é a imunoterapia, um tipo de tratamento que fortalece e estimula o sistema imunológico do paciente a atacar algum inimigo, usando várias técnicas diferentes. Esse método é usado para tratar alguns tipos de câncer e apresenta resultados promissores para outras doenças.

Nenhuma dessas ideias é nova, diga-se, mas, testadas isoladamente, não funcionaram. A combinação, porém, talvez vingue.
No estudo da Unifesp, que envolveu dezenas de pessoas, um único voluntário, conhecido apenas como “paciente de São Paulo”, ficou com níveis indetectáveis do vírus por um ano e meio depois desse combo de terapias, mesmo sem tomar o coquetel. Depois de 18 meses, o HIV voltou a dar as caras – ou seja, ele não foi curado. Mesmo assim, a remissão de longo prazo surpreendeu. Outros dois pacientes também tiveram o vírus controlado por alguns meses.
Agora, os pesquisadores brasileiros pretendem continuar nesta linha de pesquisa, tentando adaptar a estratégia para maior eficácia. Outros grupos de pesquisa mundo afora exploram métodos parecidos.
Por exemplo: um estudo publicado no fim de 2025 na revista Nature mostrou que pesquisadores de São Francisco, na Califórnia, conseguiram fazer com que sete pacientes ficassem indetectáveis por meses após uma combinação de técnicas sofisticadas de imunoterapia; um dos voluntários testou negativo por 18 meses antes do vírus voltar a dar as caras.
Além desses esforços, há outros sete casos de pessoas que tiveram curas definitivas da infecção. O método usado, porém, não é aplicável em larga escala. Você pode entendê-lo nesta outra reportagem.

Enquanto os esforços para a cura avançam aos poucos, o lenacapavir, o cabotegravir e a PrEP oral já são mais que realidade, prontos para serem aplicados – basta os governos, empresas e a sociedade civil se mobilizarem para isso. De certa forma, a ciência já fez o seu papel. Resta agora criar condições para que suas descobertas se concretizem em vidas salvas.
Contribuíram com a reportagem: Alexandre Naime Barbosa, professor da Faculdade de Medicina da Unesp de Botucatu e coordenador científico da Sociedade Brasileira de Infectologia, e Daniela Santoro Rosa, professora de Imunologia da Unifesp
Fonte: abril










