Texto Maria Clara Rossini | Design Caroline Aranha
A
Lefty’s é uma marca americana de produtos para canhotos. Ela fabrica a “versão esquerda” de tesouras, abridores de lata e itens de jardinagem. Destros representam 90% da população mundial – o que fez com que alguns objetos do dia a dia tenham sido pensados apenas para quem usa a mão direita.
Mas os clientes da Lefty’s precisam ficar ligados: a loja vende objetos que funcionam seja qual for a mão dominante. São lápis com a frase “canhotos arrasam” e canecas cuja estampa não fica virada para o rosto do canhoto (que é o que acontece com canecas normais). São alterações bacanas, mas
não essenciais.
Diferenciar um item útil (como a tesoura) de um indiferente (um lápis) é importante para que o canhoto faça valer o seu dinheiro. Mas essa distinção também reflete uma propriedade fundamental da química: a quiralidade. A tesoura é um objeto quiral, pois sua versão espelhada diverge da original. O lápis, não.
O termo “quiralidade” vem do grego kheir, que significa “mão”. Esse é o exemplo quiral por excelência, já que a mão direita é a versão espelhada da esquerda.
Coloque uma mão uma por cima da outra, com as costas delas viradas para cima, e você vai perceber que elas não se encaixam. Agora imagine um lápis, na vertical, na frente do espelho. O lápis espelhado cabe perfeitamente no objeto original.
Essa diferença entre coisas quirais e não quirais vale até em escalas minúsculas. Algumas moléculas são como mãos e tesouras, enquanto outras são como lápis. Esse entendimento foi revolucionário para a química, vital para estudar a origem das moléculas terrestres e para fabricar medicamentos seguros.
Moléculas são ambidestras
A descoberta da quiralidade teria sido o feito mais importante da vida do francês Louis Pasteur se ele não fosse, também, o pai da microbiologia.
No século 19, Pasteur demonstrou que muitas doenças são causadas por microrganismos. Além disso, ele investigou, aos 26 anos, as bases da geometria molecular do vinho.
Durante o processo de fermentação, é comum que cristais de ácido tartárico, formados a partir do açúcar da uva, se acumulem na cuba de vinho. Quando esse ácido é produzido em laboratório, no entanto, ele interage com a luz de maneira distinta (apesar de se tratar da mesma substância). Por séculos, ninguém soube o motivo. Por que uma molécula produzida de forma natural seria diferente daquela feita em laboratório?
Ao examinar a versão de laboratório do ácido com um microscópio, Pasteur verificou que havia dois formatos de cristais distintos, sendo um a versão espelhada do outro. Com muita delicadeza (e paciência), ele usou uma pinça para separar os dois tipos de cristais.
Depois, ao iluminar cada tipo de molécula, ele percebeu que um dos cristais polarizava (“entortava”) as ondas de luz no sentido horário, enquanto o outro as “entortava” no sentido anti-horário. O ácido tartárico feito em laboratório, então, entortava para ambos os lados. Pasteur também analisou a forma natural do ácido – mas só encontrou cristais que entortavam para a direita.
A experiência de Pasteur foi uma reprodução em escala macroscópica (afinal, ele pescou os cristais com uma pinça) daquilo que existe a nível molecular. Às versões espelhadas de uma mesma molécula damos o nome de enantiômeros.
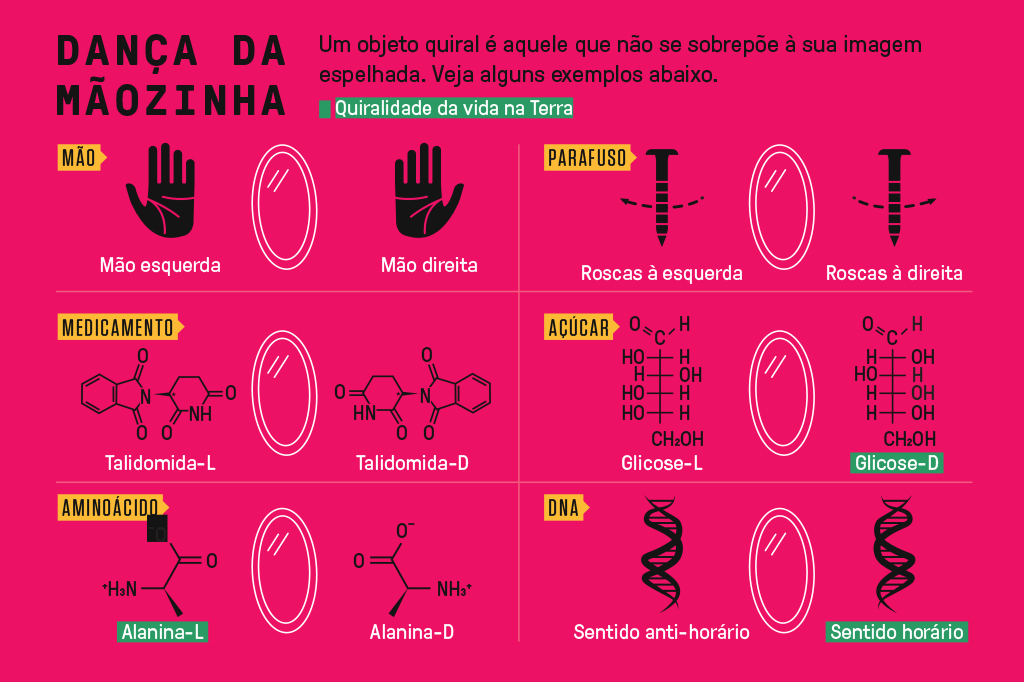
Ora, se os cristais de ácido tartárico interagem com a luz de formas diferentes, então os enantiômeros de uma molécula também têm propriedades diferentes? Sim – e é aí que está o pulo do gato.
Os enantiômeros podem ter efeitos drasticamente opostos, em especial no corpo humano. Os receptores nas nossas células funcionam no modelo “chave e fechadura”, em que a quiralidade importa. Imagine tentar abrir a porta de casa com uma chave invertida: não dá.
Essa característica é vital para a indústria farmacêutica. Um comprimido de ibuprofeno, por exemplo, contém 50% de moléculas levógiras (polarizam a luz para a esquerda) e 50% de moléculas dextrógiras (polarizam para a direita). É o que chamamos de mistura racêmica. Apenas as moléculas dextrógiras abrem a fechadura das células, causando o efeito anti-inflamatório. As outras não fazem bem nem mal – só estão no corpo a passeio.
Via de regra, a síntese de moléculas em laboratório resulta em misturas racêmicas. Os fabricantes poderiam separar as moléculas do medicamento, fazendo um comprimido mais concentrado. Mas esse é um processo caro e complexo. Vale mais deixar os dois tipos de moléculas misturados ali.
Isso funciona bem para o ibuprofeno. Em outras moléculas, no entanto, certos enantiômeros podem causar consequências graves para a saúde.
Um caso emblemático é o da talidomida. Ela era vendida nos anos 1950 e 1960 como sedativo e remédio para enjoo. Esse era o efeito da molécula dextrógira – a molécula levógira está associada à malformação fetal quando ingerida durante a gestação. E pior: quando metabolizada, a molécula dextrógira se converte
na levógira.
É por isso que gestantes não podem tomar talidomida de forma alguma. Só que, na época, a farmacêutica alemã Grünenthal não sabia disso, pois não havia testado a droga em mulheres grávidas. Durante os primeiros anos no mercado, muitas futuras mães usaram o medicamento para lidar com os sintomas de enjoo. Milhares de bebês nasceram com encurtamento dos membros. No Brasil, pelo menos 700 casos foram registrados (1).
Estudar os efeitos de cada quiralidade é peça–chave para criar medicamentos seguros. Só que separar essas moléculas sempre foi um desafio bastante caro. Não à toa, o Prêmio Nobel de Química de 2001 foi para o grupo de pesquisadores que desenvolveu métodos para sintetizar apenas um enantiômero em vez de uma mistura racêmica.
Mas, se é tão difícil separar os dois tipos de moléculas no laboratório, como é que a fermentação do vinho (que Pasteur estudou lá no século 19), um processo natural, só gera ácido tartárico dextrógiro? É a partir dessa pergunta que nasce um dos maiores mistérios da Biologia.
A vida é destra
Como vimos até aqui, uma molécula quiral pode ser dextrógira (entortar a luz para a direita) ou levógira (entortar para a esquerda). Mas há mais uma camada de distinção. Pela maneira como seus átomos estão organizados (e por convenção dos químicos), essas moléculas também são classificadas como “L” ou “D” – que podemos chamar, respectivamente, de canhotas ou destras.
(Não é uma associação óbvia. Existem moléculas de mão direita que entortam a luz para a esquerda, por exemplo. Mas não precisamos nos preocupar com isso agora. Deixemos esses pormenores para o Walter White.)

As proteínas de todos os seres vivos são formadas por combinações de apenas 20 aminoácidos. Desses, 19 são moléculas quirais (a exceção é a glicina, cuja estrutura é como o lápis do início do texto). Se o mundo tivesse saído de um laboratório, esperaria-se que cada aminoácido quiral tivesse duas versões: uma de mão esquerda (L) e uma de mão direita (D).
Mas não é isso que observamos na natureza. Tudo o que é produzido por um ser vivo tende a apenas uma quiralidade. Os 19 aminoácidos quirais, por exemplo, são de mão esquerda. Já os açúcares são de mão direita. É o caso da ribose que compõe a molécula de DNA, uma estrutura de dupla hélice quase sempre torcida para a direita, como um parafuso.
(Dá para dizer que a vida como a conhecemos aqui na Terra é destra. Sorry, canhotos.)
A vida na Terra, então, é homoquiral – dá preferência a uma quiralidade em detrimento da outra. Esse viés explica o resultado encontrado por Pasteur: sendo derivado de um ser vivo (a uva), o ácido tartárico cristalizado na fermentação só gira a luz para um lado: a direita.
Por que não o contrário? O que os canhotos fizeram com a mãe natureza para receber tanto hate?
Na teoria, o inverso poderia, sim, acontecer. Nossos aminoácidos poderiam ser de direita e os açúcares, de esquerda. É possível, inclusive, que as moléculas orgânicas em outros planetas tenham quiralidade oposta às nossas.
Em 1976, a primeira missão a pousar em Marte carregava uma solução de nutrientes com dois tipos de açúcar: lactose-D (mão direita) e lactose-L (mão esquerda) (2). A ideia era oferecer um cardápio completo aos possíveis micróbios do planeta vermelho. Nós, humanos, só metabolizamos a lactose-D. Mas vai que os alienígenas gostassem da L…
Bom, o experimento foi inconclusivo, e até hoje não sabemos se existe ou já existiu vida em Marte. Mas ainda vale a pena procurar por moléculas orgânicas quirais fora da Terra: elas são a nossa melhor chance de explicar por que a vida por aqui é homoquiral. Dependendo do que encontrarmos lá fora, os resultados podem corroborar ou refutar nossas teorias.
“A proposta principal é que, antes do surgimento da vida, existia um excesso de um dos enantiômeros na Terra – por exemplo, aminoácidos-L”, diz Douglas Galante, professor do Núcleo de Astrobiologia da USP. “Esse pequeno excesso teve vantagem em relação aos outros, as reações com eles se tornaram mais frequentes. Até que se formaram as primeiras proteínas e enzimas, e isso acabou ‘fixando’ essa homoquiralidade na vida.”
Esse processo de amplificação a partir de um desbalanço inicial é bem-aceito entre a comunidade científica. A questão é como surgiu esse desbalanço, já que, quando simulamos as condições para o início da vida em laboratório, obtemos aminoácidos de ambas as quiralidades.
Uma hipótese é que a “escolha” de lado tenha sido feita em berçários estelares. O processo de formação de estrelas emite radiação ultravioleta com polarização circular – ou seja, a luz sai girando como um pião. É diferente da polarização que vimos até aqui com as moléculas quirais, que apenas entortam a direção da luz para a esquerda ou para a direita.
Os raios UV têm tanta energia que são capazes de mudar a quiralidade de uma molécula. E aí é um efeito cascata: se uma molécula tipo L prevaleceu ante a sua versão espelhada D no meio desse processo, é assim que ela continuará a aparecer nos planetas (que, sempre bom lembrar, nascem a partir das estrelas).
“É como uma mãe [o Sol] que passa a genética para as filhas”, diz Marcelo Gleiser, físico, astrônomo e professor da Universidade de Dartmouth, no Reino Unido. Se essa teoria estiver certa, as moléculas orgânicas em outros planetas e luas do Sistema Solar devem ter quiralidades semelhantes à nossa.
Gleiser dedicou parte de sua carreira acadêmica a estudar a assimetria da vida e do Universo, e até escreveu um livro sobre o tema (3). Em um artigo publicado em 2022, ele apresenta essa e outras duas teorias possíveis para a origem da homoquiralidade (4). Vamos a elas.

Vire à direita. Ou à esquerda
Uma das hipóteses apresentadas por Gleiser é de sua autoria. O astrônomo sugere que a quiralidade das moléculas talvez seja consequência de fenômenos ambientais locais, que ocorrem ao acaso. A quiralidade, segundo ele, dependeria das interações químicas com o meio ambiente, com metade de chance de formar moléculas viradas para a esquerda, e metade de chance de serem viradas para a direita.
“Esses fenômenos na Terra poderiam ser erupções vulcânicas, queda de asteroides e cometas, terremotos violentos, ou turbulência em fluidos, como as marés”, diz Gleiser. Se esse for o caso, então devemos encontrar quiralidades variadas pelo Universo. Elas dependeriam da história de cada planeta.
Ainda não existem instrumentos sofisticados o suficiente para verificar a quiralidade de moléculas a centenas de milhões de quilômetros de distância. O sonho dos pesquisadores seria coletar amostras de todos os planetas do Sistema Solar e verificá-las de perto. Se houvesse aminoácidos ali e todos fossem de esquerda, ponto para a teoria da luz UV; se fossem diferentes, ponto para a teoria dos eventos aleatórios. Fazer algo assim, no entanto, ainda está longe da realidade.
A terceira teoria é a menos aceita entre os pesquisadores da área – mas é tão instigante que vale a pena ser mencionada. Desenvolvida pelo paquistanês Abdus Salam, vencedor do Prêmio Nobel de Física de 1979, essa hipótese liga a homoquiralidade terrestre a uma assimetria intrínseca do Universo.
O Universo é canhoto
Existem quatro forças fundamentais da natureza: gravidade, eletromagnetismo, força nuclear forte e força nuclear fraca. As duas primeiras você já conhece: uma faz a bolinha cair no chão, e a outra cola o ímã na geladeira. A terceira age sobre os quarks – partículas fundamentais que compõem os prótons e os nêutrons. A quarta é responsável pelo decaimento radioativo.
As três primeiras forças apresentam algo que chamamos de simetria de paridade. Isso significa que elas valem tanto para a mão direita quanto para a mão esquerda. Quando Alice atravessa o espelho no livro de Lewis Carroll, encontra um mundo com as mesmas leis: a bola continua caindo no chão, o ímã continua grudando na geladeira. A inversão espacial não altera
essas forças.
Isso não vale para a força nuclear fraca. Ela atua principalmente sobre uma partícula fundamental chamada neutrino – que, para fins didáticos, podemos visualizar como um pião. Esse pião sempre gira para a esquerda, independentemente de em qual lado do espelho ele está. Em outras palavras, só existem neutrinos em sua forma canhota, mesmo quando tentamos invertê-los no espaço. A quarta força da natureza quebra a simetria de paridade, fazendo com que o Universo tenha um viés para a esquerda.

Essa “quebra” da física foi confirmada em 1957 . Alguns anos depois surgiu a hipótese: e se essa característica enraizada no Universo acabou influenciando a assimetria das biomoléculas terrestres? Nesse caso, é possível que todos os aminoácidos do Universo fossem virados para a esquerda, como os nossos. É uma teoria que vem sendo estudada desde então (7).
“Será que a física de partículas e a biologia formariam uma história coesa?”, questiona Fábio Rodrigues, professor do Departamento de Química Fundamental da USP. “Hoje a gente conhece apenas a história fragmentada, e por enquanto não existe nenhuma relação entre elas.”
Existem dois pontos que baixam a bola dessa teoria. O primeiro é que a força fraca não recebe esse nome à toa: em comparação à força eletromagnética, ela contribui 1018 vezes menos para a estabilidade das moléculas. Seria difícil algo tão fraquinho ter alguma influência em suas estruturas. O segundo é que as moléculas sintetizadas em laboratório não parecem estar sendo “puxadas” para um dos lados, já que elas nascem com ambas as quiralidades.
Salam propôs que a influência da força fraca tenha sido amplificada por algum processo cósmico, e que então essas moléculas tendenciosas tenham chegado à Terra. De toda forma, essa ideia ainda fica no fim da lista de probabilidades.
Há uma última explicação no pote de teorias: dois tipos de vida primitiva podem ter evoluído na Terra, uma de mão esquerda e outra de mão direita. Por algum motivo, apenas um dos lados do espelho prosperou, fazendo o outro desaparecer sem deixar descendentes vivos.
Não sabemos se organismos com aminoácidos-D e açúcares-L (o inverso do que existe hoje) sequer seriam viáveis – afinal, o único tipo de vida que conhecemos é o nosso. Esse pseudo-ser-espelhado teria surgido antes do ancestral comum a todos os organismos atuais (conhecido pelo acrônimo LUCA), que é o tataravô que você compartilha com bactérias, fungos e plantas.
Estudar as características dessa vida espelhada hipotética poderia trazer respostas sobre a origem da vida na Terra e a possibilidade de vida em outros planetas. Em um artigo publicado na Science em dezembro de 2024, 40 pesquisadores investigaram os requisitos técnicos necessários para tentar fazer bactérias espelhadas em laboratório (8). O problema é que essa poderia ser a maior ameaça já criada contra a vida na Terra.
Nosso sistema imune evoluiu para lidar com vida destra, pois é a única que existe por aqui. Bactérias opostas provavelmente passariam despercebidas pelo corpo, e aí não teríamos nenhum recurso para combatê-las. Nem nós, nem nenhum ser vivo.
Essa ainda é uma possibilidade remota – nem sequer conseguimos fazer vida do zero em laboratório, quanto mais vida espelhada. De toda forma, os autores recomendam que nenhum laboratório tente se aventurar nessa empreitada. Da próxima vez que olhar no espelho, lembre-se que a vida (e o Universo) são bem diferentes do lado de lá.
Fontes (1) Associação Brasileira de Portadores de Síndrome da Talidomida; (2) texto “A Natural Way to Stay Sweet”; (3) livro Criação Imperfeita; (4) artigo “Biological Homochirality and the Search for Extraterrestrial Biosignatures”; (5) artigo “Experimental Test of Parity Conservation in Beta Decay”; (6) artigo “A hypothesis for the asymmetric appearance of biomolecules on earth”; (7) artigo “The role of chirality in the origin of life”; (8) artigos “Technical Report on Mirror Bacteria: Feasibility and Risks” e “Confronting risks of mirror life”.
Fonte: abril